《胆囊良性疾病外科治疗的专家共识(2021版)》解读
中华医学会外科学分会胆道外科学组
中国医师协会外科医师分会胆道外科医师委员会
胆囊良性疾病主要包括胆囊结石、胆囊炎、胆囊息肉样病变、胆囊腺肌症等。目前国内外已有较多关于胆囊良性疾病外科治疗的共识或指南,但在我国,胆囊良性疾病的治疗仍存在诸多不规范之处,将许多明确符合胆囊切除术指征的胆囊良性疾病列为“保胆手术”指征。因此,中华医学会外科学分会胆道外科学组和中国医师协会外科医师分会胆道外科医师委员会修订了《胆囊良性疾病外科治疗的专家共识(2021版)》[1],以规范胆囊良性疾病的外科治疗。本共识一经发布,引起了学界广泛的关注与热议。争议的核心主要聚焦于共识中旗帜鲜明地反对采用“保胆手术”治疗胆囊良性疾病,以及将无症状的胆囊结石纳入胆囊切除术的指征范围。为此,我们对共识中的热点问题进行以下解读。
一、共识的修订背景
目前,我国胆囊良性疾病外科治疗的不规范主要表现在对具有潜在高危胆囊癌因素的胆囊良性疾病未能及时实施规范的胆囊切除术,甚至行“保胆取石”“保胆取息肉”“胆囊部分切除术”等保胆手术,不仅会导致胆囊结石相关并发症(急性胆囊炎、穿孔、继发性胆总管结石、胆管炎、胰腺炎等)[2],还会延误胆囊癌的诊断和治疗,造成严重后果。因此,对胆囊良性疾病的治疗,亟需凝聚共识,形成规范,以预防相关并发症、降低胆囊癌发生率、节约经济成本等。
(一)胆囊良性疾病与胆囊癌的发生密切相关
胆囊癌是胆道系统常见的恶性肿瘤,具有发病隐匿、侵袭性强、进展迅速、易发生淋巴结转移等特点,预后极差,5年总体生存率不足5%。胆囊癌多由胆囊良性疾病转变而来,对具有胆囊癌高危因素的胆囊良性疾病患者及时实施规范的胆囊切除术,可明显减少胆囊癌的发生。因此,对胆囊癌的策略应是“防重于治”。《胆囊癌诊断和治疗指南(2019版)》[3]将胆囊癌发病相关危险因素分为确定危险因素和可能危险因素,其中胆囊结石、胆囊息肉样病变、胆囊慢性炎症及“保胆取石”术后胆囊为确定危险因素,而先天性胰胆管汇合异常、胆囊腺肌症、胆道感染、肥胖与糖尿病、年龄和性别、原发性硬化性胆管炎、遗传学和基因突变、吸烟及化学暴露为可能危险因素。
从流行病学特征来看,胆囊良性疾病发生率高的地区和国家,则胆囊癌的发生率亦高,二者呈正相关。以胆囊结石为例,在全球范围内,胆囊结石的高发区域与胆囊癌的高发区域相重叠,南美智利、北欧地区、北美地区及印第安人种的胆囊结石发生率高于其他区域或人种,而这些区域和人种的胆囊癌发生率亦高于其他区域或人种[4, 5]。据2021年Lancet报道,全球胆囊癌发生率呈缓慢下降趋势,但我国的胆囊癌发生率却不降反升。2021年WHO国际癌症研究机构(https://gco.iarc.fr/)公布的数据显示,全球2020年胆囊癌的新发病数量约为11万,其中我国胆囊癌新发数量为28 923例,占全球的24.9%,其中中晚期比例高达80%[6]。
(二)规范的胆囊切除术是其他胆囊癌高发地区发生率下降的重要原因
自1980年开始,随着胆囊切除术尤其是腹腔镜胆囊切除术(laparoscopic cholecystectomy,LC)在胆囊癌高发国家和地区,如智利、日本、韩国、欧美地区等的逐步开展和普及,使这些曾经的胆囊癌高发国家和地区的胆囊癌发生率出现明显的下降趋势[6]。多项研究结果显示,LC的数量与胆囊癌的发病率呈负相关[7, 8, 9, 10]。在美国,每769例胆囊切除手术可能预防1例胆囊癌的发生,而在胆囊癌发生率较高的印度北部地区,每67例胆囊切除手术即可预防1例胆囊癌的发生,可见胆囊切除手术的开展与降低胆囊癌发生率具有极为密切的关系[11]。同样在曾经胆囊癌发生率最高的智利,2006年制定了卫生健康计划实施预防性胆囊切除术,2002—2014年智利胆囊癌的全年龄死亡率由12/10万降至7.1/10万,而在35~49岁年龄组中下降趋势最明显,由4.5/10万降至1.8/10万,且这个趋势在2006年前后显著[12]。
综上所述,随着胆囊切除术的规范开展,以往胆囊癌高发地区的胆囊癌发生率已低于我国,并呈逐年下降趋势。而我国胆囊癌发生率逐年升高,且以中晚期为主(上海市1991年胆囊癌的标准化发生率为男性2.8/10万,女性3.6/10万;2000年升至男性3.8/10万,女性5.4/10万,同比升高了30%)[13]。提示该现象与我国胆囊良性疾病的治疗不规范相关。因此,规范胆囊良性疾病的规范治疗迫在眉睫,对存在胆囊癌高危因素的胆囊良性疾病及时施行规范的胆囊切除术,是有效阻断胆囊炎-癌转化、预防胆囊癌发生的重要措施。
二、胆囊良性疾病外科治疗的基本原则(推荐1~3)
自1882年Langenbuch医师成功实施了第1例胆囊切除术以来,该术式经过了百余年的临床实践,其安全性和有效性已获得广泛认同,国内外指南与共识均将其作为胆囊良性疾病的标准治疗手段,其中LC已逐步被公认为是胆囊良性疾病治疗的金标准。早在胆囊切除手术出现之前的数百年里,胆囊切开缝合及切开取石等即有开展。在胆囊切除手术开展之初,遭到部分学者的强烈反对和质疑,直至结石导致胆囊癌变理论的提出,并发现保胆取石术后结石复发率高等问题,胆囊切除术逐步取代了保胆取石术,成为治疗胆囊结石的主流术式。目前,保胆取石术在国外众多胆囊良性疾病治疗共识与指南中未再被提及,但在国内仍有医院开展并推广保胆手术,并出现了被冠以“新式保胆手术”的腹腔镜联合胆道镜取石、内镜保胆取石等治疗方式。
(一)保护胆囊,而非保留胆囊
黄志强院士指出“保护胆囊或保留胆囊?这是两个完全不同的观念——我个人不赞成保留胆囊的观念,我赞成保护胆囊的观念”[14]。保留胆囊和保护胆囊的一字之差代表的意义完全不同。在我国保胆取石相关的指南中,其适应证包括胆囊充满型结石、胆囊颈部结石嵌顿、胆囊萎缩等。保留这些病变胆囊并不是保护胆囊,其致病的温床仍存在,必然会在一定时间内再次导致疾病的发生,“一个功能丧失的胆囊,类似于一个装满石子、污泥的盲袋,一个不时发生感染的盲袋,一个纤维增厚、丧失功能、流通不畅的淤塞湖,这样的胆囊该不该保留?不该!”黄志强院士这句话明确指出了病变的胆囊绝不可以保留。
(二)保胆手术既不能改变胆囊结石的成因,亦不能规避胆囊癌的风险
1.“保胆取石”不能祛除结石成因:胆囊结石发病机制仍未明晰,目前认为主要与胆固醇代谢异常、促成核因子作用及胆囊排空功能障碍等多种因素相关。每例患者出现胆囊结石的原因与进程不完全相同,单纯取石不能去除结石成因,术后结石复发率高。有长期随访的临床研究结果显示,保胆取石术后的总体结石复发率为20%~41.5%,随访时间均在1年以上,甚至出现了随访时间越长,复发率越高的趋势[15, 16, 17, 18]。国内少数开展保胆手术的医师同样也进行了临床研究,但普遍存在随访时间短、随访率低、缺少客观结果、统计方法有待改进、不符合循证要求等问题[19, 20, 21],研究质量不高。另外,目前的药物治疗亦无法避免术后结石复发。
2.“保胆取石”无法消除癌变机制:在胆囊结石的病因及疾病发展过程中,胆囊慢性炎症始终贯穿疾病全程,由于慢性炎症会导致局部黏膜DNA损伤,进而活化胆囊的自身修复机制,使得黏膜细胞处于增生的状态,从而加速了“化生-异型增生-癌”这一过程[22];目前无证据表明“保胆取石”能够逆转术后胆囊慢性炎症病程,消除“炎-癌转化”机制;更无法消除胰胆管汇合异常、原发性硬化性胆管炎、慢性肠炎等胆囊癌变因素。
3.卫生经济学无获益:“保胆取石”术后由于结石复发率高,多数患者需长期口服熊去氧胆酸等药物。而复发后患者往往需要再次手术,增加了患者的痛苦及医疗费用。
4.部分“保胆取石”术后患者的临床症状并未消失:胆囊结石相关的并发症如胆总管结石、胆管炎、胆源性胰腺炎等仍会发生。
5.对胆囊腺瘤性息肉行“保胆取息肉”危害极大:保胆取息肉无法去除息肉蒂部,避免息肉复发。而最大径>10 mm的腺瘤性息肉已有癌变可能,但多为早期(Tis、T1期),单纯胆囊切除术即可能获得长期生存。对此类患者行“保胆取息肉”术,将不可避免地使含有癌细胞的胆汁外溢至腹腔,极易导致肿瘤腹腔种植转移,危及患者生命。
(三)“保胆手术”也可能发生相关并发症
与LC相比,行“保胆手术”的患者同样面临全身麻醉和手术的相关风险(胆囊穿孔、胆瘘、感染、切口并发症等)。有学者指出,镜下取石操作可能造成胆囊黏膜损伤,有时还需撕开或切开黏膜取石,胆囊亦需建立创口并缝合或夹闭,这些局部创伤、炎症及瘢痕可能成为结石复发甚至癌变的始动因素[23]。在取石、碎石过程可能导致小结石进入胆总管,以及由胆道镜的冲洗液导致整个胆道系统压力失衡,均可诱发胆管炎和胰腺炎。此外,胆汁和冲洗液外溢对腹腔造成的污染可导致广泛的腹腔粘连,尤其是通过内镜保胆的金属夹造成的异物反应和粘连更为严重。许多保胆取石术后结石复发的患者,再次行胆囊切除术将面临更大的困难和风险。许多保胆手术相关研究对其相关并发症避而不谈,保胆手术的近远期并发症需进一步统计和公开。
(四)“保胆手术”后胆囊是胆囊癌的危险因素
由于胆囊结石的形成机制及炎症并未消除,“保胆手术”无法逆转术后结石复发及胆囊慢性炎症病程,无法消除“炎-癌转化”机制。而且,“保胆手术”会导致具有胆囊癌高危因素的患者延误行胆囊切除手术的时机,增加胆囊癌发生的风险。
(五)保胆取石相关研究文章质量不高
2010年以来,中国知网共发表1 457篇保胆取石相关文章,其中多数文章的研究质量不高,难以作为高级别的临床证据。而在PubMed中共有37篇保胆取石相关文章,其中26篇来自我国,而另11篇来自国外的文章中多将保胆取石手术作为接受胆囊切除手术有高风险的患者在行胆囊置管引流术之后的替代方案[24, 25, 26]。“保胆手术”这一由国外学者首创,并与胆囊切除术并驾齐驱百年余,已被逐渐抛弃,成为标准治疗方案外的辅助备选方案,它既未比现有的胆囊切除手术更安全,又无法避免术后结石复发等所导致的炎症、再次手术及卫生经济学相关问题,更是诱发胆囊癌发生的危险因素。因此,为了规范胆囊良性疾病的治疗,共识重点强调了反对“保胆手术”的观点,以期改变国内这一治疗现状。
三、胆囊结石的外科治疗(推荐4)
长期以来,对于无症状的胆囊结石是否需行手术切除,一直存有争议。既往版本的国内外指南与共识对于有症状的胆囊结石建议手术切除,但对于无症状的胆囊结石,建议以密切随访为主。考虑到胆囊结石作为明确的胆囊癌的危险因素,本共识提出胆囊结石患者无论有无症状均符合胆囊切除术指征,但共识中并未要求对所有胆囊结石患者立即实施手术。在手术时机选择上需考虑患者的意愿,对暂不接受手术的无症状胆囊结石患者,应密切随访。如出现临床症状、胆囊结石相关并发症(急性胰腺炎、胆总管结石或胆管炎等)及胆囊癌相关的高危因素时,应及时实施胆囊切除术。
(一)胆囊结石是胆囊癌明确的高危因素
约85%的胆囊癌患者合并胆囊结石[27],胆囊结石患者患胆囊癌的风险是无胆囊结石人群的13.7倍,是胆囊癌明确的危险因素[28, 29]。已形成结石的胆囊,其内在的环境及平衡已遭到破坏,早期胆囊的吸收与浓缩功能可能存在,但在反复结石刺激下,其随时可能出现慢性炎症、黏膜损伤直至状态无法逆转,最终出现结石相关并发症甚至恶变。因此共识提出,胆囊结石患者即使无症状,亦符合手术指征。
(二)“无症状胆囊结石”患者真的无症状吗?
临床上很多患者对于“无症状”的定义存在偏移,其实已存在明显腹胀、隐痛等消化道症状,但尚未严重至需就医用药,甚至部分患者被初诊为“胃病”,均认为自己仍属于“无症状”胆囊结石状态,此类患者往往是胆囊癌变的高危人群。临床上常会遇到常年无主观不适的“无症状胆囊结石”患者,但一旦出现临床症状便被诊断为胆囊癌晚期,使对无症状胆囊结石仅需随访观察的策略受到质疑。主要原因是胆囊结石发生率高,保守治疗现象非常普遍,尤其是国内少数医师对“无症状胆囊结石”实施不科学的“保胆取石”手术,虽然暂时去除了结石,但胆囊内成石环境无法逆转,局部炎症情况已存在甚至经保胆手术后进一步加重,从而导致结石复发率高,胆囊癌变的风险增加。因此,本共识反对对无症状胆囊结石患者实施“保胆手术”。
四、胆囊炎的外科治疗(推荐5~8)
对于急性胆囊炎的病情,应依据临床症状、体征、实验室检查和影像学检查结果综合评估其严重程度,制订相应治疗决策并动态评估病情及效果。东京指南2018年指出,应根据其炎症程度分级,选择合理的治疗方案。共识在此基础上,结合我国治疗现状,制定了符合我国国情的外科治疗建议。原则上是早期行胆囊切除术,患者无法耐受时可考虑胆囊穿刺引流作为替代治疗方案。
慢性胆囊炎往往合并胆囊结石、胆囊壁增厚、胆囊萎缩、胆囊排空障碍等。当合并胆囊结石时,应积极手术切除胆囊。而对于无结石的慢性胆囊炎患者,应评估胆囊收缩功能,当发生胆囊排空障碍时,存在胆汁淤积并进一步成石的风险,亦是胆囊癌变的诱因,因此推荐切除胆囊。而胆囊壁增厚>3 mm、萎缩性胆囊炎等为胆囊癌的危险因素,亦应积极手术切除胆囊。
黄色肉芽肿性胆囊炎是一种特殊的胆囊炎症性疾病,发病机制尚不明确。其特征是胆囊壁含有泡沫细胞、炎症细胞及纤维组织浸润性沉积,在术前与胆囊癌极难鉴别,仔细询问患者的发病经过和行影像学检查对诊断有一定的指导作用,但需术中快速病理学检查来确诊。当术前、术中各种方法均无法排除胆囊癌时,应按照胆囊癌的治疗原则选择切除范围,并进一步进行病理学检查。
五、胆囊息肉样病变及胆囊腺肌症的外科治疗(推荐9~12)
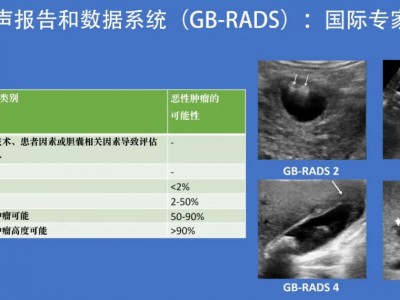
胆囊息肉样病变指影像学检查发现的所有胆囊黏膜隆起性病变的统称,包括胆固醇性息肉、腺肌症、炎性息肉、增生性息肉、腺瘤等,其检出率逐年上升[30, 31]。由于胆囊息肉的大小是腺瘤性息肉的独立相关因素,既往共识和指南均以胆囊息肉>10 mm作为胆囊切除术的指征。但临床上6~9 mm的息肉发生癌变的病例屡见不鲜,因此,息肉大小已不能单纯作为判断是否需手术治疗的指标。目前尚未见关于胆固醇性息肉癌变的报道,而腺瘤性息肉的癌变率较高。如何判断胆囊息肉性质,是决定是否行胆囊切除术的关键,现有的影像学技术可通过测及血流情况来判断是否为腺瘤性息肉。因此共识提出,将是否能测及血流作为确定手术指征的重要指标。推荐对于测及血流的胆囊息肉样病变,无论其大小,均应及时实施胆囊切除术。而对于未测及血流的胆囊息肉,再根据其大小选择合适的治疗方案。
胆囊腺肌症是胆囊壁黏膜增生性疾病,可分为局限性、节段型和弥漫型。胆囊腺肌症的癌变率约为6%[32]。不同分型的癌变率不同,局限性腺肌症的癌变率相对较低,当合并胆囊结石或分型为节段型时,其癌变风险显著增高。胆囊部分切除既不能消除胆囊腺肌症的癌变因素,还会影响胆囊功能。因此,共识对于胆囊腺肌症的患者推荐适时实施胆囊切除术,并强调术中需行快速病理学检查,以免造成胆囊癌的漏诊,同时再次明确反对对胆囊息肉样病变实施“保胆手术”,并反对对胆囊腺肌症实施胆囊部分切除术。
六、胆囊的变异和畸形(推荐13)
胆囊的变异、畸形或发育异常可导致胆汁淤积,易致胆固醇沉淀,同时影响胆囊收缩功能,最终导致胆石症。对于无症状的胆囊畸形,如无炎症改变,可考虑密切随访。而对于出现胆囊积液、扭转、结石、胆囊炎的胆囊变异和畸形,推荐手术切除胆囊。
七、胆囊切除术后会严重影响患者的生活质量吗?(推荐14)
胆囊切除术总体上是安全的,绝大多数患者并不会出现明显的临床症状。但胆囊切除术后也可能出现一些并发症,主要包括:Oddi括约肌功能障碍相关性胆源性腹痛、术后消化功能紊乱相关性腹胀和腹泻等。部分患者的症状与胆囊切除术的不规范相关,如残余小胆囊、胆囊管残留过长、继发胆总管结石等。胆管损伤是胆囊切除术后的严重并发症,虽然发生率很低,但后果严重,手术医师应给予充分重视、提高手术技能,尽量避免胆管损伤等严重并发症的发生[33]。
八、其他相关问题
(一)胆囊切除术后会导致结直肠癌发生吗?
20世纪七八十年代有学者提出,胆囊切除可能是结直肠癌的危险因素[34, 35],对公众观念造成了较大影响。近年来,有研究结果显示,消化道肿瘤,特别是右半结肠癌与胆囊结石存在相关性,而这些相关性与胆囊切除术无关[36]。2009年及2019年2篇Meta分析结果均显示,胆囊结石与结直肠癌的发病具有相关性,而胆囊切除术本身并不会增加结直肠癌的发生风险[37, 38],这可能与肠道-微生物群-肝脏的调控机制有关[39]。
(二)胆囊切除术后会增加胆总管结石的发生率吗?
国内有学者认为,胆囊切除会增加原发性胆总管结石的发病率,但支持此观点的临床研究却鲜有报道。目前国内外均缺乏该方面的大型流行病学数据,多为小样本研究,有文献显示其发生率约为1.5%[40]。另外,胆囊结石发生率升高会导致继发性胆总管结石的发生率升高[41]。
九、总结
综上所述,对符合胆囊切除指征的胆囊良性疾病患者,应适时行胆囊切除术,既能解除胆囊现存疾病的临床危害,还可降低胆囊癌的发生率,提高胆囊癌的早期诊断率和根治性切除率,改善胆囊癌患者的预后,达到对于胆囊癌“防重于治”的原则。现阶段在结石成因、形成机制及预防、炎-癌转化等问题尚未解决的情况下,“保胆手术”无法解决结石高复发率、胆囊癌变等问题。

 微信扫一扫,打赏作者吧~
微信扫一扫,打赏作者吧~